1. 简介
他是一种提供局部高洁净度工作环境通用性较强的空气净化设备,他的使用对改善工艺条件,提高产品质量和增大成品率均有良好效果。 2.3 主要特点
A.表面静电喷涂,准闭合式整体不锈钢台面,可有效防止外部气流透入,及操作异味对人体的刺激。
B.采用可调风量风机系统,轻触型开关及双速调节电压大小,保证工作区风速处于理想状态。
C.轻触型开关调节风量,保证工作区风速在要求的范围内。 3. 工艺用户需求 3.1 工作环境
4台超净工作台为洁净区,温度18—26℃,相对湿度45—65% 。 4. 机械和电器用户需求 4.1 洁净度
对于粒径≥0.5um的尘埃≤3.5颗/升(100级) 4.2 菌落数
对于粒径≤0.5个/皿·时(直径为90mm的培养皿) 4.3 平均风速 0.32~048m/s 4.4 噪音 ≤65dB 4.5 电源
220V 50Hz 4.6 外形尺寸
宽*深*高:980mm*700mm*1630mm 4.7 其他说明
工作台出风口散流板安装照明日光灯和紫外线杀菌灯。净化工作区操作面板采用透明有机玻璃制作。底部有万向脚轮,移动方便,到位后轮子可随时定位。 5. 自动控制用户需求(GMP第七十一条,附录1第七十条) 5.1 综述
超净工作台的供应商要提供设备自动控制过程的工艺描述和功能标准及操作的详细说明,自动控制需要符合EUGMP和GAMP4的要求。 5.2 安全
5.2.1自动控制系统由有生产资质的供应商提供,并有检测报告或产品合格证等
证明文件,经检测合格方可安装。
5.2.2自动控制系统应符合中G现行法律法规和行业标准的要求,安 全,可靠,并设有分级管理的安全密码。如经理级密码可调整技术参数;操作级密码不能调整参数,只能按已设定参数和流程操作等。 5.3接口(GMP第七十一条,附录1第六十四条) 5.3.1 所有接口均不影响检测全过程
5.3.2 超净工作台所有接口均设有表示用途的标识或标牌。 5.3.3 标准电脑接口,可连接打印机和电脑。
5.4技术系统要求(GMP第七十一、七十五、七十九、九十、九十一、九十二、九十三、九十四、九十五条,附录1第九、六十一、六十三、六十四、七十、七十二条)
5.4.1 应配备有适当量程和精度的量具、仪器和仪表。
5.4.2 PLC性能可靠,反应灵敏,操作方便且经过校验,良好人机界面,中文或英文显示。
5.4.3 自动控制系统维修保养方便,零配件易得。
5.4.4 培养箱配备的量具、仪器和仪表均应经过校准和检验,并提供相关记录。校准的量程范围应涵盖实际生产和检验的使用范围,所得数据准确、可靠。 5.4.5 上述校验者应具有合格校验资质,且符合G家有关规定。校准记录应当标明所有计量标准器具的名称、编号、校准有效期和计量合格证明编号,确保记录的可追溯性。
5.4.6 所有已校验的量具、仪器和仪表应贴有校验标识,并标明校验有效期。不得使用未经校准、超过校准有效期或失准的量具、仪器和仪表。 5.4.7 应提供PLC验证方法的书面文件和记录表。 5.4.8 打印机可以打印超净工作台操作时全过程
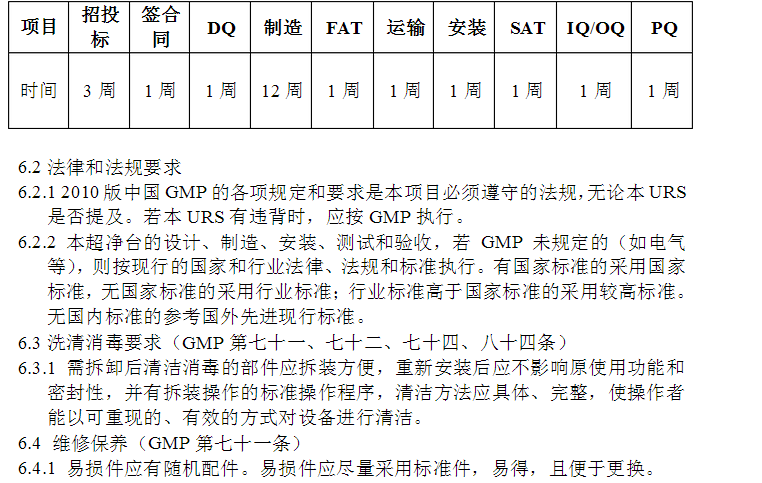
6.项目实施用户要求 6.1进度表
6.4.2 使用说明书中应明确规定润油剂的名称、型号、加注频次、加注量、加注方法和注意事项。
6.4.3 各零部件和电气应维修方便,有维修空间。
6.4.4 使用说明书中应说明故障报警时的诊断、维修方法,并有维修标准操作程序(含预防维修)。 #p#分页标题#e#
6.4.5 应有控制系统恢复启动备份软件盘。 7. 环境、健康、安全
7.1 本超净工作台应符合G家相关机器设备安全设计规范
7.2 本超净工作台应符合G家相关机器设备节能和环境控制规范,如节能高效、降噪音等。
7.3 不采用对人体健康有害的材料和加工方法。
8. 供货、服务要求(GMP第七十、七十三、八十二、八十三条,附录1第四十、六十一、六十三、六十五、七十、七十二条) 8.1 发展
本超净工作台用于检测,需要符合CGMP或其他机构(如美GFDA、中GSFDA)等的授权或批准,并且符合他们的规定。
因此合格的文件需要从项目开始时就开始准备(如材质证明等),供应商需要为这个项目进行一个周密的质量计划。
8.2 测试与验证(GMP第138、139、140、141、142、143、144、145、146、147、148、149条)
本超净工作台的供应商应进行设备进入使用阶段前的设备验证工作,这是达到设备预期要求的有效手段,这不仅是阶段交付验收,还是贯穿在整个DQ—FAT—SAT—IQ—OQ—PQ验证过程中的符合性确认工作,对每一个环节都应有执行人、复核人确认,并要求每一项符合预定的标准,若出现不符合项,需要执行《偏差处理程序》。 8.2.1 DQ,FAT,SAT 8.2.1.1 DQ
DQ应符合URS/FDS/图纸/GMP法规要求,确保FDS的设计要求满足URS和法规的要求,对FDS和URS不符合项,应与需求方协商确认。 8.2.1.2 FAT
供应商在设备出厂前应对设备进行整体测试,对制造文件详细检查,如材料、焊接、压力容器证书等。对于在IQ/OQ中无法检查的项目,应安排在FAT中进行,如自动控制功能的模拟和挑战实验等。 8.2.1.3 SAT
供应商在现场组装设备完成后应进行整体测试,确保系统能按设计要求正常运转,并对需方员工进行培训,同时准备SOP,为IQ作准备。 8.2.2 IQ/OQ/PQ 8.2.2.1 IQ
供应商应提供IQ文件和记录表,协助需方进行检查确认,如仪表与管道的检查、设备主要特性及安全特性的检查等。 8.2.2.2 OQ
供应商提供OQ文件和记录表,协助需方进行仪表的校准(控制用仪表和记录用仪表)、安全检查、报警测试、单项功能测试、整体性测试、故障诊断程序、维修自测程序、程序运行等。8.2.2.3 PQ
供应商应提供PQ文件和记录表,指导需方的PQ。 8.3 交货
8.3.1 设备的运输
8.3.1.1 应提前二周通知需方设备运输预计到达时间,以便需方提前做好接货准备工作。
8.3.1.2 设备运输前供应商应妥善包装,如设备主体和零部件应先用塑料薄膜包裹,并固定在底座上,重要部位用塑料泡沫等材料保护、垫实,木箱,防水外包装,外包装上有明显标识,标明设备名称、型号、数量、发货人、收货人、毛重、起吊位置、开箱位置等。 8.3.1.3 随车送货单
应包括的内容:发货日期、发货人、货物名称、型号、数量、外包装形式、毛重、收货人等。 8.3.1.4 运输方式
门对门货运汽车防雨运输,即货运汽车直接送达需方厂区内。 8.3.2 安装
8.3.2.1 供应商负责在货到后一周内派专业技术人员到需方工厂安装,并承担差旅费和食宿费。
8.3.2.2. 安装所需专用工具和检测仪器、仪表由供应商负责解决。
8.3.3 文件(GMP第150、151、154、155、156、157、158、159、160、161、163条)
供应商应尽量提供原版文件,无法提供原版文件时可提供复印件并加盖公章。供应商应提供(但不限于)下列文件一式二份: (1) 中华人民共和G医疗器械注册证
(2) 中华人民共和G特种设备制造许可证(压力容器) (3) 政府主管部门颁发的计量许可证 (4) 美GASME认证的CE认证证书
(5) G际DNV组织颁发的ISO9000和13485质量体系认证证书 (6) 质量保证计划
(7) 设备说明和工艺流程说明
(8) 设备相关图纸(安装图、结构图、电气图、电器原理图等) (9) 设备部件清单及参数
(10)电气和电器部件的技术文件 (11)清洁和钝化流程和报告 (12)接触流程部件的材质报告 (13)表面处理证书
(14)硬件规格和系统结构 (15)触摸屏程序 (16)FAT方案及报告 (17)SAT方案及报告 (18)IQ文件 (19)OQ文件 (20)PQ文件 (21)用户手册
(22)维护手册 (23)备件清单
(24)产品质量保证书 (25)产品质检合格证书
8.3.4 培训(GMP第26、27、28条) 供应商负责在SAT、IQ和OQ过程中对需方员工进行理论和操作及维护培训,并对维修人员进行设备预防性维修和故障诊断及维修的培训。 8.4 可交货的报价单
供应商的报价单**少要包含如下信息: ①超净工作台工艺流程图/安装操作图 ②设备部件的规格 #p#分页标题#e#
③标有设备部件位置和主要尺寸的布局图 ④材料的标准和处理的标准(制造者的标准) ⑤主要部件的尺寸和重量 ⑥交货时间
⑦现场安装调试的时间 ⑧做IQ、OQ验证的时间 ⑨操作培训的时间
⑩电源和其它配套公用设施参数 8.5 售后服务
设备保修期**少一年。终身维修服务,维修反应时间24小时内。 9. 附件